|
|
|
|
|
|
|
ΕΛΟΝΟΣΙΑ >
Πληροφορίες για Επαγγελματιες > Εργαστηριακή Διάγνωση
|
|
ΕΛΟΝΟΣΙΑ
|
|
|
Η εργαστηριακή διάγνωση της ελονοσίας περιλαμβάνει την ανίχνευση του παρασίτου ή των αντιγόνων/ προϊόντων αυτού στο αίμα του ασθενούς.[1, 2]
Οι απαιτήσεις μια διαγνωστικής δοκιμασίας είναι η ευαισθησία, η ειδικότητα, η ευκολία στην εφαρμογή και το προσιτό κόστος.[1]
Οι διαθέσιμες επί του παρόντος διαγνωστικές τεχνικές μπορούν να χωριστούν σε τρεις κατηγορίες:
I. Μικροσκοπική εξέταση
II. Ανοσολογικές τεχνικές
III. Μοριακές τεχνικές
Ι. Μικροσκοπική εξέταση
Υπάρχουν δύο είδη, η κλασσική μελέτη επιχρίσματος αίματος υπό το οπτικό μικροσκόπιο και η νεότερη μέθοδος ανίχνευσης παρασίτων υπό μικροσκόπιο υπεριώδους ακτινοβολίας- φθορισμού.
Μελέτη επιχρίσματος αίματος
Αποτελεί το χρυσό κανόνα (gold standard) για τη διάγνωση της ελονοσίας.[1, 2, 3, 4]
Τα βήματα που ακολουθούνται είναι τα εξής: λήψη δείγματος περιφερικού αίματος από τον ασθενή, δημιουργία παχείας σταγόνας και λεπτής στιβάδας αίματος επί του πλακιδίου, χρήση χρώσης Giemsa και στη συνέχεια εξέταση, με το οπτικό μικροσκόπιο, των ερυθρών αιμοσφαιρίων για παράσιτα ελονοσίας.[1, 2]
Μελέτη παχείας σταγόνας: δεν περιλαμβάνει διαδικασία μονιμοποίησης, γεγονός το οποίο έχει σαν αποτέλεσμα την αιμόλυση· έτσι, τα μόνα ανιχνεύσιμα στοιχεία επί του πλακιδίου είναι τα λευκοκύτταρα και τα παράσιτα της ελονοσίας. Από την άλλη μεριά, η λύση των ερυθροκυττάρων μπορεί να επιφέρει παραμόρφωση των πλασμωδίων, γεγονός που δυσκολεύει την ταυτοποίησή τους. Επομένως, το επίχρισμα παχείας σταγόνας μελετάται κυρίως για τον υπολογισμό της παρασιταιμίας έχοντας μια ευαισθησία της τάξης των 5- 10 παρασίτων/ μl.[2]
Μελέτη λεπτής στιβάδας: σε αντίθεση με την παχιά σταγόνα, υπόκειται σε μονιμοποίηση με μεθανόλη. Έτσι, ο εξεταστής έχει τη δυνατότητα να ταυτοποιήσει το είδος του παρασίτου, να αναγνωρίσει διάφορες μορφές του παρασίτου (γαμετοκύτταρα, σχιστοζωίτες) και να υπολογίσει το μέγεθος της παρασιταιμίας. Η ευαισθησία της μεθόδου είναι 200 παράσιτα/ μl.[2]
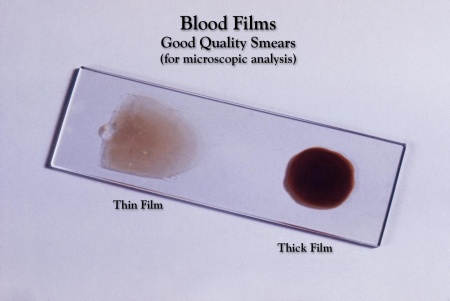
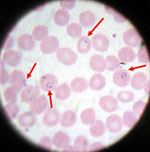
Η Εικόνα 1 που ακολουθεί, απεικονίζει ένα πλακίδιο με παχεία σταγόνα και λεπτή στιβάδα αίματος ενώ η Εικόνα 2 το πώς φαίνονται τα παράσιτα εντός των ερυθροκυττάρων στη φάση της μικροσκόπησης.
 |
|
Εικόνα 1, επίχρισμα- παχεία και λεπτή σταγόνα
[Πηγή: CDC]
|
Εικόνα 2, μολυσμένα ερυθρά υπό το μικροσκόπιο
[Πηγή: CDC]
|
Πλεονεκτήματα:
- Φθηνή μέθοδος
- Προσφέρει στον εξεταστή τη δυνατότητα να εκτιμήσει το μέγεθος της παρασιταιμίας και να διακρίνει το είδος του πλασμωδίου.[1, 2, 3]
Μειονεκτήματα:
- Η διαγνωστική ακρίβεια εξαρτάται τόσο από την ποιότητα του επιχρίσματος και του διαθέσιμου εξοπλισμού όσο και από τις ικανότητες του μικροσκόπου και της ώρας που αφιέρωσε ο τελευταίος στη μελέτη του πλακιδίου.[2, 4]
- Ακατάλληλη μέθοδος για επιδημιολογικές μελέτες μεγάλης κλίμακας.
- Ψευδώς θετικό αποτέλεσμα: μπορεί να οφείλεται σε λανθασμένη προετοιμασία του επιχρίσματος οπότε προκύπτουν κυτταρικά θραύσματα που μπορεί να εκληφθούν ως παράσιτα. Ακόμη και φυσιολογικά στοιχεία του αίματος, όπως τα αιμοπετάλια, μπορεί να επιφέρουν σύγχυση στη διάγνωση.[3]
- Ψευδώς αρνητικό αποτέλεσμα: συνήθως σχετίζεται με χαμηλή παρασιτική ‘πυκνότητα’ ή μειωμένο αριθμό πεδίων που μελετήθηκαν από τον εξεταστή.[3]
Εκπαιδευτική Παρουσίαση για την Εργαστηριακή Διάγνωση της Ελονοσίας - ΕΣΔΥ
Quantitative Buffy Coat (QBC)
Αυτή η νεότερη μέθοδος συνίσταται σε μικροσκοπική εξέταση υπό υπεριώδες φως και μετά από φυγοκέντρηση στιβάδας ερυθροκυττάρων, χρωματισμένων με ακριδίνη. Η όλη διαδικασία λαμβάνει χώρα σε ένα γυάλινο σωληνάριο μικροαιματοκρίτη ο οποίος είναι εσωτερικά επιστρωμένος με ακριδίνη και οξαλικό κάλιο. Το σωληνάριο γεμίζεται με 55- 65 μl αίματος και φυγοκεντρείται με αποτέλεσμα τα στοιχεία του αίματος να διαχωρίζονται με βάση την πυκνότητά τους δημιουργώντας ζώνες όπως φαίνεται στην Εικόνα 3.[2]
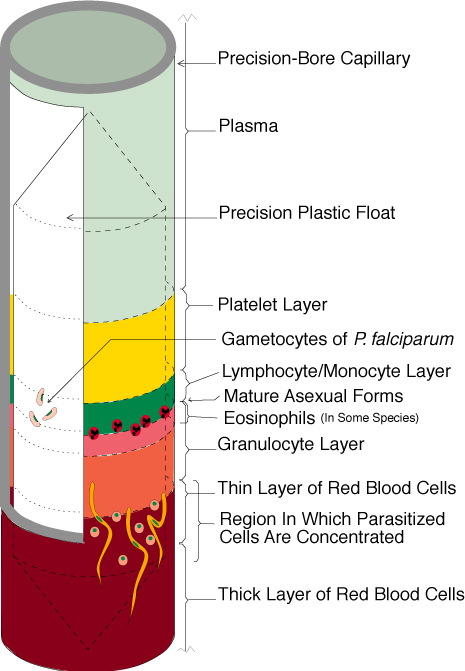
Εικόνα 3, qbc, ζώνες που δημιουργούνται με τη φυγοκέντρηση
[Source: qbcdiagnostics.com]
Στη συνέχεια, με τη χρήση ενός μικροσκοπίου υπεριώδους ακτινοβολίας, παρατηρούνται τα φθορίζοντα παράσιτα στη διαχωριστική επιφάνεια μεταξύ ερυθρών και λευκών αιμοσφαιρίων όπως φαίνεται στην Εικόνα 4 που ακολουθεί.[2]
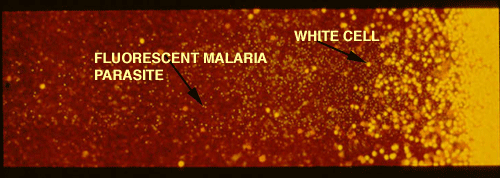
Εικόνα 4, φθορίζοντα παράσιτα υπό μικροσκόπιο υπεριώδους ακτινοβολίας
[Source: en.impact-malaria.com]
Πλεονεκτήματα:
- Ευκολότερη και ταχύτερη σε σχέση με την κλασική μικροσκόπηση
Μειονεκτήματα:
- Ακριβός εξοπλισμός
- Αδύνατη η ταυτοποίηση του είδους πλασμωδίου και η ακριβής μέτρηση των παρασίτων[2]
ΙΙ. Ανοσολογικές τεχνικές
Τεχνικές βασιζόμενες στην ανίχνευση αντισώματος
(i) Δοκιμασία έμμεσου φθορισμού αντισωμάτων (Indirect Fluorescent Antibody Test, IFAT)
Το αντιγόνο αποτελείται από μολυσμένο αίμα δεσμευμένο στις 12 θέσεις ενός πλακιδίου. Σε κάθε θέση τοποθετείται μια σταγόνα του αραιωμένου προς έλεγχο ορού και μετά από επώαση προστίθεται διάλυμα αντι- ανθρώπινης ανοσοσφαιρίνης σεσημασμένης με ισοθειοκυανική φθοριοσεΐνη που περιέχει κυανούν του Evans ως χρωστική αντίθεσης. Όταν τα πλακίδια στεγνώσουν, εξετάζονται σε μικροσκόπιο φθορισμού. Το αντίσωμα στον ορό αντιδρά με το αντιγόνο του παρασίτου και η αντίδραση της αντι- ανθρώπινης ανοσοσφαιρίνης με το αντίσωμα φαίνεται με το φθορισμό των παρασίτων όπως δείχνει η Εικόνα 5.[5]
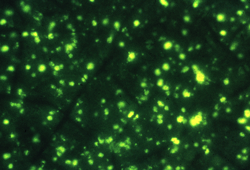
Εικόνα 5, μικροσκόπηση φθορισμού
[Source: en.impact-malaria.com]
Τα μειονεκτήματα της τεχνικής αυτής είναι ότι απαιτεί την ύπαρξη μικροσκοπίου φθορισμού αλλά και ιδιαίτερων ικανοτήτων από τον εξεταστή.[5]
(ii) Δοκιμασία ενζυμικής ανοσοαπορρόφησης (Enzyme- Linked Immunosorbent Assay, ELISA)
Η μέθοδος αυτή χρησιμοποιεί ένα διαλυτό αντιγόνο παρασίτου ελονοσίας επιστρωμένο στα τοιχώματα ενός τρυβλίου μικροτιτλοποίησης (Εικόνα 6). Στη συνέχεια εγχύεται στις θέσεις του τρυβλίου δείγμα αίματος του εξεταζόμενου προκειμένου για ανίχνευση αντισωμάτων. Αν η δοκιμασία είναι θετική, το αντίσωμα δεσμεύει το αντιγόνο με αποτέλεσμα μια ορατή χρωματική αλλαγή. Όταν η διαδικασία είναι αρνητική, δηλαδή επί απουσίας αντισωμάτων, τότε δεν παρατηρείται καμία χρωματική αλλαγή στο υπόστρωμα.[5]
Εικόνα 6, τρυβλίο τεχνικής ELISA
[Source: en.impact-malaria.com]
Τεχνικές βασιζόμενες στην ανίχνευση αντιγόνου
Δοκιμασία ταχείας διάγνωσης (Rapid Diagnostic Test, RDT)
Το γνωστό rapid test είναι μια μικρή συσκευή η οποία μπορεί να ανιχνεύσει αντιγόνα ελονοσίας σε μια μικρή ποσότητα αίματος (5μl) με ανοσοχρωματογραφία (:αλλαγή χρώματος της απορροφητικής ταινίας νιτροκυτταρίνης[6]) με τη χρήση μονοκλωνικών αντισωμάτων στραμένων κατά παρασιτικών αντιγόνων[3]. Συγκεκριμένα, το αίμα αφήνεται να «τρέξει» πάνω στην ταινία νιτροκυτταρίνης μετά από ρίψη διαλύματος Buffer και το αποτέλεσμα που παρατηρούμε προκύπτει από το χρωματισμό των γραμμών στις αντίστοιχες θέσεις των μονοκλωνικών αντισωμάτων με τα οποία αντέδρασε το αντιγόνο που περιέχεται στο αίμα. Ανάλογα με το αντιγόνο- στόχος, οι γραμμές των αντισωμάτων επί της ταινίας μπορούν να έχουν συνδυασμούς αντισωμάτων για τα παρακάτω αντιγόνα:
- HRP2 (Histidine Rich Protein- 2): είναι μια πρωτεΐνη που παράγεται από κυτταρικά στάδια της ασεξουαλικής φάσης αναπαραγωγής και από τα γαμετοκύτταρα του P. Falciparum και η οποία εκφράζεται στη μεμβράνη των ερυθροκυττάρων. Ενίοτε, η πρωτεΐνη αυτή παραμένει στο αίμα του ασθενούς ακόμη και για εβδομάδες μετά από επιτυχές θεραπευτικό σχήμα . (Ευαισθησία: ανίχνευση παρασιταιμίας> 50 παράσιτα/ μl). Το αντίστοιχο rapid test ονομάζεται PfHRP2.[4]
- Αλδολάση του πλασμωδίου: είναι ένα ένζυμο της γλυκολυτικής οδού του παρασίτου που εκφράζεται από όλα τα πλασμώδια της ελονοσίας (pan malaria antigen, PMA ονομάζεται το αντίστοιχο rapid test). [4]
- LDH (γαλακτική αφυδρογονάση): είναι κι αυτό ένα ένζυμο της γλυκολυτικής οδού που παράγεται από μορφές του ασεξουαλικού σταδίου αναπαραγωγής του παρασίτου και απελευθερώνεται από τα προσβεβλημένα ερυθρά αιμοσφαίρια. (Ευαισθησία: ανίχνευση παρασιταιμίας> 100 παράσιτα/ μl). Το αντίστοιχο rapid test ονομάζεται pLDH. [4]
Η ταινία του PfHRP2 RDT έχει 2 γραμμές, μία είναι η γραμμή ελέγχου (Control) που πιστοποιεί την εγκυρότητα του τεστ και μία για το ζητούμενο αντιγόνο. Η ταινία του PfHRP2/PMA και του pLDH διαθέτει 3 γραμμές, μία για τον έλεγχο εγκυρότητας και 2 για τον αντιγόνο του P. Falciparum και τα αντιγόντα των μη falciparum πλασμωδίων.
Η αλλαγή του χρώματος στη γραμμή ελέγχου είναι απαραίτητη για την εγκυρότητα της εξέτασης. Η αλλαγή χρώματος μόνο σε αυτή, ερμηνεύεται ως αρνητικό αποτέλεσμα.
Στο PfHRP2 rapid test, η αλλαγή χρώματος και στις 2 γραμμές ερμηνεύεται ως θετικό για λοίμωξη από P. Falciparum (Εικόνα 7).
Στα PfHRP2/PMA και pLDH rapid tests, η αλλαγή χρώματος στη γραμμή ελέγχου και στη γραμμή των μη falciparum, ερμηνεύεται ως μόλυνση από πλασμώδιο εκτός του falciparum ενώ αλλαγή χρώματος και στις 3 γραμμές, σημαίνει την παρουσία λοίμωξης από P. Falciparum (είτε ως μονολοίμωξη είτε ως συλλοίμωξη με άλλα στελέχη) όπως φαίνεται στην Εικόνα 7. Ως εκ τούτου, οι μικτές λοιμώξεις από falciparum δεν μπορούν να διαφοροδιαγνωστούν από αμιγείς μολύνσεις από falciparum. [4]
Εικόνα 7, RDT με 2 και 3 γραμμές, (+) για P. falciparum
[Source: springerimages.com]
Πλεονεκτήματα:
- Δεν απαιτείται ηλεκτρισμός κι έτσι μπορεί να γίνει στο πεδίο (in the field), ιδιαίτερα στις περιπτώσεις όπου δεν είναι δυνατή η παροχή μικροσκόπησης.
- Απλή μέθοδος και στην πραγματοποίηση και στην ερμηνεία με δυνατότητα αποτελέσματος εντός 15- 30 λεπτών.
- Δυνατότητα για έρευνα επιδημιών της νόσου αλλά και για έλεγχο των ταξιδιωτών με πυρετό που επιστρέφουν από ενδημικές χώρες.[3, 6]
- Η δοκιμασία HRP-2 RDT προσφέρει ευαισθησία > 90% για το P. falciparum και η δοκιμασία LDH RDT > 95%.[3]
Μειονεκτήματα:
- Χαμηλή ευαισθησία στην ανίχνευση ασυμπτωματικών ασθενών και ειδικά σε χαμηλά επίπεδα παρασιταιμίας.[2, 4, 6]
- Διασταυρούμενες αντιδράσεις με αυτοαντισώματα (όπως ο ρευματοειδής παράγοντας στην περίπτωση του HRP-2 RDT).[2, 3]
- Ψευδώς θετικά αποτελέσματα (γαμετοκυτταραιμία, εμμένουσα παρασιταιμία ασεξουαλικού σταδίου κάτω από το όριο ανίχνευσης μικροσκόπησης).[2]
- Ψευδώς αρνητικά αποτελέσματα (γενετική εξάλειψη ή μεταλλαγή του αντιγόνου hrp- 2).[2, 3]
Συμπερασματικά, ένα rapid test θα πρέπει πάντα να ακολουθείται από μια επιβεβαίωση του αποτελέσματος με μικροσκόπηση[2], μια αρνητική δοκιμασία για να αποκλειστεί το ενδεχόμενο χαμηλής παρασιταιμίας και μια θετική δοκιμασία για επιβεβαίωση του είδους του πλασμωδίου που ανιχνεύει το rapid test και για ποσοτικοποίηση των μολυσμένων ερυθρών αιμοσφαιρίων.[2, 4]
III. Μοριακές τεχνικές
Αλυσιδωτή αντίδραση πολυμεράσης (Polymerase Chain Reaction, PCR)
Η χρήση της PCR προσφέρει τη δυνατότητα ανίχνευσης των τεσσάρων βασικών πλασμωδίων (P. vivax, P. malariae, P. ovale, P. falciparum) με ευαισθησία 10 φορές υψηλότερη σε σχέση με εκείνη της μικροσκόπησης.[2]
Παρά το γεγονός ότι μια τέτοια μέθοδος μπορεί να ανιχνεύσει «υπομικροσκοπικές» παρασιταιμίες, δεν υπάρχει ακόμη αντίστοιχη εγκεκριμένη μέθοδος από τον Παγκόσμιο Οργανισμό Τροφίμων και Φαρμάκων για τη διάγνωση της ελονοσίας ή για τον έλεγχο των υποψηφίων αιμοδοτών. Το μόνο σίγουρο είναι ότι περαιτέρω έρευνα θα ακολουθήσει προκειμένου τέτοιου τύπου μέθοδοι να εφαρμόζονται ευρέως.[7]
Πλεονεκτήματα
- Υψηλή ευαισθησία και ειδικότητα.[1]
- Νέες τεχνολογίες (NAT, LAMP) προσφέρουν δυνατότητα χαμηλότερου κόστους και υψηλότερης ευαισθησίας και ειδικότητας και για τα 5 είδη πλασμωδίων που θεωρούνται παθογόνα για τον άνθρωπο από τον ΠΟΥ (Παγκόσμιο Οργανισμό Υγείας).[7, 8]
- Ανίχνευση μικτής λοίμωξης [1]
- Ανίχνευση λοίμωξης από στελέχη ανθεκτικά στα ανθελονοσιακά[1]
- Αυτοματισμός, υψηλή ταχύτητα[1]
- Δυνατότητα ποσοτικού προσδιορισμού παρασίτων και διάκρισης στελέχους[1]
Μειονεκτήματα
- Πολύ ευαίσθητη για κλινική χρήση[1]
- Ακατάλληλο για χρήση στο πεδίο (in the field)[1]
- Ακριβή[1]
- Απαιτητική από τεχνική άποψη[1, 8]
Αναφορές:
[1] David Warrell, Herbert Gilles, 2002, Essential Malariology 4th edition, Boston: Oxford University Press.
[2] Ιστοσελίδα για την ελονοσία Malaria site, www.malariasite.com
[3] Chansuda Wongsrichanalai, Mazie J. Barcus, Sinuon Muth, Awalludium Sutamihardja and Walther H. Wernsdorfer, A review of malaria diagnostic tools: microscopy and rapid diagnostic test, American Journal of Tropical Medicine and Hygiene, 2007, pp. 119- 127.
[4] Ιστοσελίδα του Αμερικανικού Κέντρου Ελέγχου & Πρόληψης Νοσημάτων (CDC), www.cdc.gov
[5] Impact malaria site, www.en.impact-malaria.com
[6] WHO, The use of Malaria Rapid Diagnostic Tests 2nd Edition, 2004, WHO site
[7] Babita Mahajan, Hong Zheng, Phuong Thao Pham, Mary Y. Sedegah, Victoria F. Majam, Namita Akolkar, Maria Rios, Isaac Ankrah, Parnor Madjitey, George Amoah, Ebenezer Addison, Isabella A. Quakyi and Sanjai Kumar, Polymerase chain reaction- based tests for pan- species and species-specific detection of human plasmodium parasites, Transfusion, 2011.
[8] Rashad Abdul- Ghani, Abdulsalam M. Al- Mekhlafi, Panagiotis Karanis, Loop- mediated isothermal amplification (LAMP) for malarial parasites of humans: Would it come to clinical reality as a point- of- a- care test?, 2012, Acta Tropica, 122; 233- 240
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Αυτός ο ιστότοπος έχει παραχθεί για τις ανάγκες του «Ειδικού προγράμματος ελέγχου για τον ιό του Δυτικού Νείλου και την ελονοσία, ενίσχυση της επιτήρησης στην ελληνική επικράτεια» και αντιπροσωπεύει τις απόψεις των συντακτών του. Οι απόψεις αυτές δεν έχουν υιοθετηθεί ή εγκριθεί με οποιοδήποτε τρόπο από την Ειδική Υπηρεσία του τομέα Υγείας & Κοινωνικής Αλληλεγγύης και της Ευρωπαϊκής Επιτροπής και δεν πρέπει να εκλαμβάνονται ως θέσεις του Υπουργείο ή της Επιτροπής. Η Ειδική Υπηρεσία δεν εγγυάται την ακρίβεια των στοιχείων που περιλαμβάνονται στον παρόντα ιστότοπο, ούτε αποδέχεται την ευθύνη για οποιαδήποτε χρήση των πληροφοριών αυτών.
|
|
|
|
 |
|